Условие:
Для реакции H2 + J2 ↔ 2HJ выполните следующее задание:
1) Сформулируйте принцип Ле-Шателье.
2) Определите, как влияют изменения давления на положение равновесия реакции.
3) Составьте выражение для константы равновесия и вычислите её значение.
Равновесные концентрации реагирующих веществ (с, моль/л) приведены под соответствующими химическими формулами в уравнении реакции.
Решение:
Дано:
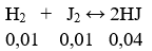
Найти: Кр - ?
1. При изменении условий протекания реакции (температуры, давления, концентрации какого либо вещества), химическое равновесие нарушается, происходит смещение равновесия. Направление этого смещения подчиняется принципу Ле-Шателье:
Если на систему, находящуюся в состоянии химического равновесия, оказать какое-либо воздействие, то равновеси...
