Условие:
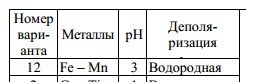
Два металла находятся в контакте друг с другом (табл. 14). Определите, какой металл из данной пары будет подвергаться коррозии, и выполните следующие задания:
1. Определите термодинамическую возможность коррозии это-го металла с указанной деполяризацией при Т = 298 К и заданном значении рН. Концентрация ионов металла в водном растворе равна 0,001 моль/дм3. Парциальные давления водорода и кислорода име-ют следующие значения: PН2 = 5·10–7 атм, PО2 = 0,21 атм.
2. Напишите электронные уравнения процессов, протекающих при коррозии металла на анодном и катодном участках.
3. Подберите анодное и катодное покрытия для защиты данного металла от коррозии. Составьте уравнения процессов, происходящих при нарушении покрытия в растворе соляной кислоты.
Решение:
Сравним значения стандартных электродных потенциалов железа и марганца
(Fe2+/Fe) = -0,44В
(Mn2+/Mn) = - 1,18В
В данной паре марганец более активный металл (т.к. (Mn2+/Mn) = - 1,18В (Fe2+/Fe) = -0,44В), поэтому он будет подвергаться коррозии.
Коррозия, как самопроизвольный процесс, протекает в том случае, если энергия Гиббса реакции имеет отрицательное значение (∆G 0).
Коррозия с водородной деполяризацией. Рассчитаем потенциал окислителя, учитывая что рН = 3, PН2 = 5107 атм
