Условие:
ЭДС гальванического элемента Zn | ZnCl2 (C = 0,0102 M) | AgCl, Ag равна 1,155 В. Определите стандартный потенциал электрода Cl-|AgCl, Ag, если средний коэффициент активности ZnCl2 в указанном растворе равен 0,714, а стандартный потенциал электрода Zn2+|Zn равен – 0,758 В.
Дано: C(ZnCl2) = 0,0102 M; E = 1,155 В; f±( ZnCl2) = 0,714; φ0(Zn2+|Zn) = - 0,758 В.
Найти: φ0(Cl-|AgCl, Ag) - ?
Решение:
Е = (Cl-|AgCl, Ag) - (Zn2+|Zn),
где (Cl-|AgCl, Ag) потенциал катода, В;
(Zn2+|Zn) потенциал анода, В.
Потенциал цинкового электрода вычислим по уравнению Нернста:
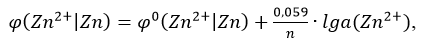
где 0(Zn2+|Zn) стандартный электродный потенциал цинкового электрода, равен - 0,758 В;
п число электронов, участвующих в анодном процессе Zn2+ + 2е Zn0, равно 2;
а(Zn2+) активность ионов Zn2+, моль/л.
Активность ионов равна
...
