Условие:
Какая масса бромной воды потребуется для окисления 30,4 г сульфата железа 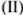 в сернокислом растворе, если в 100 г воды
в сернокислом растворе, если в 100 г воды 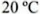 растворяется 3,58 г брома?
растворяется 3,58 г брома?
Дано:
mFeSO4 = 30.4 г mBr2 = 3.58 г
Найти: m - ?
Решение:
Составим уравнение реакции:
FeSO4 + Br2 + H2SO4 = Fe2(SO4)3 + HBr
2* | Fe2+ - e- = Fe3+ железо восстановитель, окисляется с +2 до +3
1*| Br20 + 2e- = 2B...
