Какие из перечисленных металлов будут растворяться при обычных условиях в растворах реагентов? Напишите уравнения соответствующих реакций, составьте уравнения электронного баланса, уравняйте приведённую реакцию, дайте названия процессам и реагентам.
- Химия
Условие:
1. Какие из перечисленных металлов будут растворяться при обычных условиях в растворах реагентов, отмеченных в таблице знаком «+»?
2. Напишите уравнения соответствующих реакций, составьте уравнения электронного баланса, уравняйте приведённую реакцию, дайте названия процессам и реагентам (укажите процессы окисления и восстановления, окислитель и восстановитель).
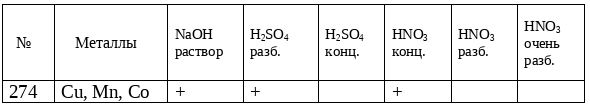
Решение:
Металлы, расположенные левее водорода, способны вытеснять его из растворов кислот, условно называемых кислотами - неокислителями, т.е. окисляться катионом водорода такой кислоты. Следовательно, с H2SO4 (разб.) будет взаимодействовать Mn и Со. Разб. H2SO4 не окисляет Cu:
Mn + H2SO4 (разб .) MnSO4 + H2.
Восстановитель | Mn0 - 2e- Mn+2 -процесс окисления.
Окислитель |2H+ + 2e- H2 - процесс восстановления.
Co + H2SO4 (разб .) CoSO4 + H2.
Восстановитель | Co0 - 2e- Co+2 -процесс окисления.
Окислитель |...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства