Условие:
Константа равновесия реакции между двуокисью углерода СО2(г)+Н2(г) 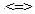 СО(г)+ Н2О(г)при 8500С=1. Исходная концентрации веществ равнялись СН2=0,2 моль/л; ССО2=0,8 моль/л. Рассчитайте, при какой концентрации водорода установится равновесие?
СО(г)+ Н2О(г)при 8500С=1. Исходная концентрации веществ равнялись СН2=0,2 моль/л; ССО2=0,8 моль/л. Рассчитайте, при какой концентрации водорода установится равновесие?
Решение:
Дано:
Кр=1
C0(H2)=0,2 М
С0(CO2)=0,8 М
Найти:
[H2]-?
CO2+H2=CO+H2O
Выражение константы равновесия:
