Условие:
Металлическое изделие необходимо электрохимическим способом покрыть серебром. Предложить схему процесса. Какое количество электричества (в числах Фарадея) надо пропустить через раствор электролита, чтобы получился слой серебра массой 1.08 г?
Решение:
Для покрытия металлического изделия электрохимическим способом серебром необходимо провести электролиз соли серебра , например нитрат серебра. При этом катодом будет металлическое изделие, требующее покрытия, а анод - активный -серебряный
Ag NO3 = Ag+ + NO3-
(-) Kатод Ag+, H2O
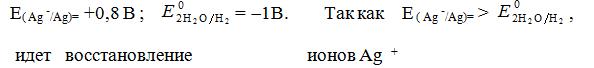
K ( - ) Ag+ + ē = Ag
(+) Aнод (Ag) NO3- H2O
1,8 B. Нитрат -ионы не разряжаются E= +0,8 B
