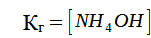Условие:
Напишите уравнения гидролиза хлорида аммония в молекулярной и ионной форме. Вычислите константу и степень гидролиза NH4Cl в 0,1 М растворе.
Решение:
Дано:
С(NH4Cl) = 0,1 M,
Kb = 1,76*10-5
Найти: Kг(NH4Cl) = ?,
h(NH4Cl) = ?
1) Запишем уравнения гидролиза хлорида аммония:
NH4Cl + H2O = NH4OH + HCl,
NH4+ + H2O = NH4OH + H+.
Высвобождаются ионы водорода, среда раствора хлорида аммония кислая.
2) Для расчета константы гидролиза составим выражение для Кг реакции. Согласно закону действия масс: