Условие:
Навеску железной руды массой 0,2500 г перевели в раствор. Содержащееся в растворе Fe (III) восстановили до Fe(II) и оттитровали его. На титрование израсходовали 28,55 мл 0,1050 н. раствора перманганата калия 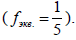
Рассчитать массовую долю железа в руде.
Решение:
Для определения железа используется метод окислительно-восстановительного
титрования. При титровании протекает реакция:
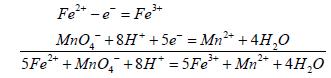
Учитывая, что один ион Fe(II) отдает один электрон (z = 1, fэкв. = 1), эквивалент железа Fe2+. Ион MnO4 принимает пять электронов (z = 5, fэкв. = ), эквивалент перманганата калия
