Условие:
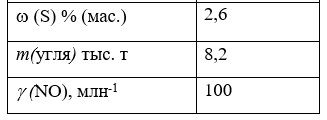
Оцените молярное соотношение и общую массу диоксида серы и оксида азота, поступающих в атмосферу в течение суток с выбросами тепловой электростанции, работающей на угле. Содержание серы в угле равно w % (мас.). В сутки на станции сжигается т тыс. т угля. Концентрация оксида азота в газовых выбросах составляет g млн-1. Для сжигания угля используется стехиометрически необходимое количество воздуха. В расчетах принять, что уголь состоит из углерода и содержит в качестве примеси только серу.
Решение:
Диоксид серы в выбросах отходящих газов при сжигании топлива появляется в результате окисления соединений серы, присутствующих в исходном топливе. Процесс может быть представлен уравнением:
S + O2 = SO2
Количество серы, сжигаемое на станции за сутки, составит:
m (S) = m(угля) ∙ (S) = 8200 ∙ 0,026 = 213,2 (т / сут),
где m(S) и m (угля) - массы серы и угля, сжигаемого на станции за сутки;
(S) массовая доля серы в угле.
Количество молей диоксида серы, образующейся в результате сгорания угля, равно количеству молей серы, содержащейся в угле:
n(SO2) = n(S) = m(S)/ M(S), где M(S) молярная масса серы, г...
