Условие:
Рассчитать ЭДС элемента, состоящего из марганцевой пластинки, погруженной в 0,01 М раствор Mn(NO3)2 и свинцовой, погруженной в 0,01 М раствор соли Pb(NO3)2. Вычислить ΔG и указать возможность работы такого элемента.
Решение:
Чтобы определить какой металл выступает в роли анода, а какой в роли катода необходимо сравнить их стандартные электродные потенциалы:
0Mn2+/Mn=-1,18 B 0Pb2+/Pb=-0,13 B
Поскольку 0Mn2+/Mn 0Pb2+/Pb, то марганцовый электрод анод, а свинцовый электрод катод.
Схема гальванического элемента:
A(-)Mn|Mn(NO3)2(0,001 M)║Pb(NO3)2(0,001 M)|Pb (+)K
Процессы на электродах:
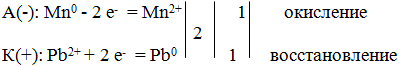
Суммарная токообразующа...
