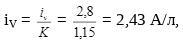Условие:
Анодная медь, подвергающаяся электролитическому рафинированию, содержит 99,35 % Сu, 0,16 % Ni, 0,017 % As. В процессе анодного растворения в электролит переходит 75 % Ni и 65 % As. Объёмная плотность тока в ваннах cоставляет 2,8 А/л. Объём электролита, вне ванн равен 15 % от объёма электролита в ваннах. Анодный выход по току 96 %.
Определить продолжительность электролиза, при которой будет достигнуто предельное содержание примесей в электролит. Предельное содержание для никеля составляет 18 г/л, а для мышьяка 3,0 г/л. Рассчитать минимальный объём электролита, который необходимо выводить из оборота, чтобы не допустить превышение предельного содержания примесей в ходе процесса электролиза.