Условие:
По данным, приведенным в табл. 5, составьте:
а) гальванический элемент, состоящий из двух окислительно-восстановительных электродов: A, B|Pt и C, D|Pt;
б) запишите электрохимические реакции на электродах, суммарную электродную реакцию процесса, протекающего в элементе;
в) вычислите константу равновесия этой реакции и ЭДС гальванического элемента. Активности веществ в растворе aA, aB, aC и aD приведены в табл. 5.
Таблица 5
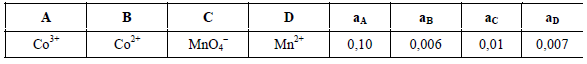
* Активность ионов водорода в растворе равна 0,1
