Условие:
Пользуясь значениями энтальпии реакции MgO(т) + Al2O3(т) = =(MgAl2)O4(т), рассчитайте ΔS0 и ΔG0 для данной химической реакции. По полученным значениям ΔG0, определите возможность самопроизвольного протекания реакции в неизолированной системе при стандартных условиях. Энтальпия химической реакции ΔН0реакц = -39 кДж.
Решение:
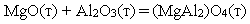
Энтропии образования веществ, участвующих в этой реакции:
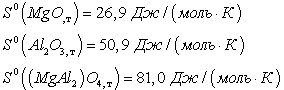
Воспользуемся четвертым следствием из закон...
