Решение задачи
При анализе магнитного железняка взяли навеску массой 0,6 г. После соответствующей обработки был получен осадок, весовая форма которого Fe2O3 имела массу 0,4326 г. Вычислите массовую долю
- Химия
Условие:
При анализе магнитного железняка взяли навеску массой 0,6 г. После соответствующей обработки был получен осадок, весовая форма которого Fe2O3 имела массу 0,4326 г. Вычислите массовую долю Fe3O4 в анализируемом образце.
Решение:
Дано: 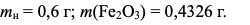
Найти: (Fe3O4) - ?
Для решения задачи необходимо вычислить молярные массы Fe2O3 и Fe3O4.
М(Fe2O3) = 55,84∙2 + 16,00∙3 = 159,68 (г/моль).
М(Fe3O4) = 55,84∙3 + 16,00∙4 = 231,51 (г/моль).
Найдём массу Fe3O4, которая содержалась в исходной навеске магнитного желез...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э