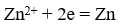Решение задачи
При электролитическом осаждении всего цинка из 0.4 дм3 раствора ZnCl2 на аноде выделилось 5.6 дм3 хлора (н.у.). Рассчитайте массу цинка и молярную концентрацию исходного раствора. Составьте уравнения электродных процессов.
- Химия
Условие:
При электролитическом осаждении всего цинка из 0.4 дм3 раствора ZnCl2 на аноде выделилось 5.6 дм3 хлора (н.у.).
Рассчитайте массу цинка и молярную концентрацию исходного раствора. Составьте уравнения электродных процессов.
Решение:
На катоде одновременно протекают процессы восстановления ионов Zn2+ и молекул H2O, так как значения электродных потенциалов их близки по величине
Zn0 = -0.76 B, H,OH0 = -0.83 B при pH = 14.
На аноде происходит окисление ионов хлора, молекулы воды не окисляются из-за большого перенапряжения кислорода.
| K(-): |
|
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э