Решение задачи
Рассчитать константу равновесия (Кс) реакции N2(г) + 3H2(г)= 2NH3(г), если исходные концентрации N2 и H2 соответственно равны 0,4 и 2,24 моль/л и к моменту равновесия прореагировало 20% исходного количества азота. Записать математическое выражение Кр и
- Химия
Условие:
Рассчитать константу равновесия (Кс) реакции N2(г) + 3H2(г)= 2NH3(г), если исходные концентрации N2 и H2 соответственно равны 0,4 и 2,24 моль/л и к моменту равновесия прореагировало 20% исходного количества азота.
Записать математическое выражение Кр и определить совпадают ли Кр и Кс численно.
Дано:
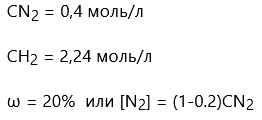
Найти:
k = ?
Решение:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э