Условие:
Разберите работу гальванического элемента, который описывается схемой
Ni | Ni(NO3)2 || AgNO3 | Ag,
СNi2+ = 10-2 моль/л; СAg+ = 10-1 моль/л.
Напишите электронные уравнения анодного и катодного процессов, составьте ионное уравнение окислительно-восстановительной реакции в гальваническом элементе. Вычислите его ЭДС.
Решение:
Выпишем из справочника значения стандартных электродных потенциалов:
Е0Ni2+ = -0,250 В; Е0Ag+ = +0,799 В.
Вычислим потенциалы электродов по уравнению Нернста.
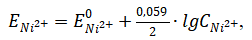
где Е0Ni2+ - стандартный электродный потенциал никеля, равен 0,250 В;
2 число электронов, которое отдает никель в процессе Ni0 2e Ni2+;
СNi2+ - концентрация раствора соли никеля, равна 10-2 моль/л.
