Решение задачи
Разложение на поверхности золота при высоких температурах протекает по уравнению 2N2O(г) 2N2(г) + O2(г). Константа скорости данной реакции равна 5×10–4 л/(моль×мин) при 1173 К. Начальная концентрация 3,2 моль/л.
- Химия
Условие:
Разложение на поверхности золота при высоких температурах протекает по уравнению 2N2O(г) 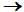 2N2(г) + O2(г). Константа скорости данной реакции равна 5×10–4 л/(моль×мин) при 1173 К. Начальная концентрация 3,2 моль/л.
2N2(г) + O2(г). Константа скорости данной реакции равна 5×10–4 л/(моль×мин) при 1173 К. Начальная концентрация 3,2 моль/л.
Определите скорость реакции при данной температуре в начальный момент и в тот момент, когда разложится 25% N2O.
Решение:
Уравнение реакции:
2N2O(г) = 2N2(г) + O2(г)
Константа скорости k = 5104 л/(мольмин).
C0 = 3,2 моль/л.
Из размерности константы скорости видно, что данная реакция 2 порядка.
Скорость реакции 2 порядка:
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э