Решение задачи
Сернистый газ, содержащийся в дымовых газах промышленных предприятий, можно использовать для получения серы. Какой объем сероводорода необходим для улавливания SO2, образующегося при сжигании 1 т
- Химия
Условие:
Сернистый газ, содержащийся в дымовых газах промышленных предприятий, можно использовать для получения серы. Какой объем сероводорода необходим для улавливания SO2, образующегося при сжигании 1 т высокосернистого угля с содержанием серы 3,7%? Какая масса серы при этом получится?
Решение:
При сжигании угля сера окисляется до SO2:
S + O2 = SO2
Запишем выражение закона эквивалентов для этой реакции.
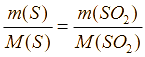
Масса серы в угле:
m(S) = m(угля) (S) = 1 = 0,037 т, или 37 кг
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
S
А
Б
В
Г
И
К
М
П
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
Р
С
Т
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства
Ф
Э