Составьте электронные уравнения и укажите, какой процесс – окисления или восстановления происходи при следующих превращениях: А) Mn3+→ Mn2+, MnO2→ Mn2+, ( MnO4)2-→(MnO4)-, Mn2+→( MnO4)2-
- Химия
Условие:
Составьте электронные уравнения и укажите, какой процесс – окисления или восстановления происходи при следующих превращениях:
А) Mn3+→ Mn2+, MnO2→ Mn2+, ( MnO4)2-→(MnO4)-, Mn2+→( MnO4)2-
Б) На основании электронных уравнений расставьте коэффициенты электронно – ионным методом в уравнениях реакций, идущих по схемах
Cd + H2SO4( k)=CdSO4 + SO2 + Н2О
KMnO4 + Н3 АsO3 +Н2SO4 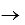 MnSO4 +Н3АsO4 + K2SO4 + Н2О
MnSO4 +Н3АsO4 + K2SO4 + Н2О
Решение:
А) Mn3+ +е Mn2+ процесс восстановления
Mn4+ O2 +2е Mn2+, процесс восстановления
( Mn6+ O4)2- -е (Mn7+ O4)-, процесс окисления
Mn2+ -4е ( Mn6+ O4)2- процесс окисления
Б) Cd + H2SO4( k)=CdSO4 + SO2 + H2O
Cd0 -2e = Cd2+ | процесс окисления
S6+ O42- +2e + 4H+ = SO2 + 2H2O процесс восстановления
Cd + SO42- + 4H+ = Cd2+ + SO2 + 2 H2O
Cd + 2H2SO4( k)= CdSO4 + SO2 + 2H2O
Cd -восстановитель
H2SO4-окислитель
Н3 АsO...
Похожие задачи
Не нашел нужную задачу?
Воспользуйся поиском
Выбери предмет
- Правоохранительные органы
- Пожарная безопасность
- Парикмахерское искусство
- Природообустройство и водопользование
- Почвоведение
- Приборостроение и оптотехника
- Промышленный маркетинг и менеджмент
- Производственный маркетинг и менеджмент
- Процессы и аппараты
- Программирование
- Право и юриспруденция
- Психология
- Политология
- Педагогика
- Трудовое право
- Теория государства и права (ТГП)
- Таможенное право
- Теория игр
- Текстильная промышленность
- Теория вероятностей
- Теоретическая механика
- Теория управления
- Технология продовольственных продуктов и товаров
- Технологические машины и оборудование
- Теплоэнергетика и теплотехника
- Туризм
- Товароведение
- Таможенное дело
- Торговое дело
- Теория машин и механизмов
- Транспортные средства