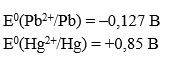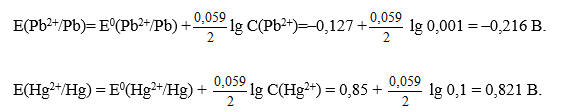Условие:
Составьте схему гальванического элемента из металлических электродов М1 и М2, находящихся в растворах собственных солей с концентрациями ионов С1 и С2. Напишите уравнения электродных процессов и токообразующей реакции. Рассчитайте ЭДС при 298 К двумя способами.
Металл 1 — Pb
Металл 2 — Hg
C(Pb2+) = 0,001 моль/л
C(Hg2+) = 0,1 моль/л