Условие:
Термохимическое уравнение реакции сгорания ацетилена:
2С2Н2 + 5О2 → 4СО2 + 2Н2О + 2610 кДж
Сколько теплоты выделится, если будет израсходовано:
а) 13 г ацетилена; б) 1,12 л ацетилена; в) 1 моль ацетилена.
Решение:
Запишем термохимическое уравнение реакции сгорания ацетилена:
2С2Н2 + 5О2 4СО2 + 2Н2О + 2610 кДж
Как видно из уравнения реакции, в ходе сгорание 2-х моль ацетилена образуется 2610 кДж энергии.
Следовательно, при сгорании одного моль ацетилена образуется:
Qсг = 2610 / 2 = 1305 кДж/моль
а) Вычислим количество вещества ацетилена в 13 г:
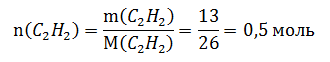
Вычислим ...
