Условие:
Установите природу вещества, содержащегося в реакторе, если навеску этого вещества m = 0,5 г при температуре t oC спарили в объем V = 1 л при давлении Р. Обратите внимание, что Р выражено в килопаскалях.
Вычислите молекулярную массу вещества.
Химический состав вещества определите по молекулярной массе и плотности жидкости. Напишите структурную формулу выбранного вещества.
t =870C, P = 18,7 кПа, Рраб. = 57 Па (Т =298 К), tок = 5250С.
4. Приведите объем пара в п. 3 к нормальным условия.
5. Определите плотность пара при н.у.
6. В воздухе над реактором парциальное давление вещества А при температуре 250С равно Рраб. Рассчитайте мольно-объемную концентрацию вещества А в воздухе и сравните ее с ПДК в воздухе, сделайте взвод о необходимости очистки вентиляционных газов от испаряющегося из реактора вещества.
7. Представьте результаты в виде.
8. В вентиляционные выбросы попадает вещество А. Очистку выбросов от вещества А осуществляют каталитическим окислением его кислородом воздуха при температуре tок. Напишите уравнения реакции.
9. На основании значений энтальпий образования веществ 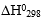 определите тепловой эффект реакции окисления
определите тепловой эффект реакции окисления 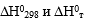 с учетом агрегатного состояния всех участников реакции при температутре t.
с учетом агрегатного состояния всех участников реакции при температутре t.
10. Рассчитайте стандартное химическое сродство для изучаемой реакции окисления при температуре 298 К и Т К.
11. Результаты вычислений внесите в таблицу.
Решение:
1. Молярная масса вещества:
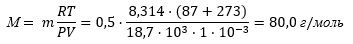
2. Вещество твердое. Это вещество этиленхлоргидрин.
3. Структурная формула вещества:
Сl-CH2-CH2-OH
4. Находим объем пара при н.у.:
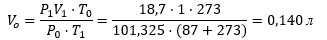
5. Плотность пара при н.у.:
= m/V =0,5/0,14...
