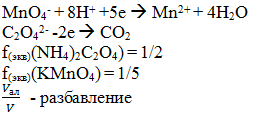Условие:
В мерной колбе емкостью 250 см3 растворили 0,7112 г химически чистого оксалата аммония (NH4)2C2O4. Какой объем перманганата калия с титром 0,00142 г/см3 пойдет на титрование 25 см3 полученного раствора оксалата аммония? Напишите уравнения реакций в ионно-электронной и молекулярной формах.
Дано:
V = 250 см3
m((NH4)2C2O4) = 0,7112 г
T (KMnO4) = 0,00142 г/см3
Vал = 25 см3
V(KMnO4) = ?
Решение:
5(NH4)2C2O4 + 2KMnO4 + 8H2SO4 = 2MnSO4 + 10CO2 + K2SO4 + 5(NH4)2SO4 + 8H2O