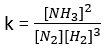Условие:
В начальный момент протекания реакции 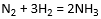 концентрации были равны, моль/ дм3: азота – 1,5; водорода – 2,5; аммиака – 0. Каковы концентрации азота и водорода при концентрации аммиака, равной 0,5 моль/дм3 ? Запишите выражения для скорости реакции и для константы равновесия. Как можно увеличить выход аммиака?
концентрации были равны, моль/ дм3: азота – 1,5; водорода – 2,5; аммиака – 0. Каковы концентрации азота и водорода при концентрации аммиака, равной 0,5 моль/дм3 ? Запишите выражения для скорости реакции и для константы равновесия. Как можно увеличить выход аммиака?