Условие:
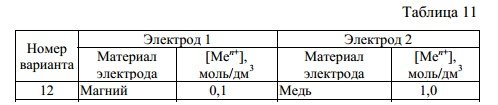
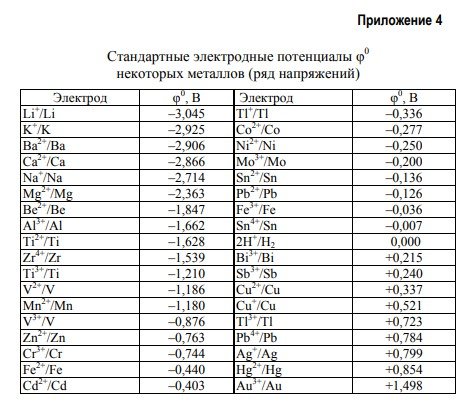
В табл. 11 указаны материалы электродов и концентрации ионов металла в растворе электролита[Mе n+] (моль/дм3). Значения стандартных электродных потенциалов металлов приведены в прил. 4.
Используя эти данные, выполните следующие задания:
1. Составьте схему гальванического элемента.
2. Рассчитайте электродные потенциалы анодного и катодного
процессов, вычислите ЭДС гальванического элемента.
3. Напишите уравнения процессов, протекающих на электро-дах. Составьте суммарное уравнение реакции, лежащей в основе работы гальванического элемента.
Решение:
Дано:
(Mg2+/Mg) = -2,363В
(Cu2+/Cu) = 0,337В
[Mg2+] = 0,1 моль/л
[Cu2+] = 1 моль/л
Электродный потенциал магниевого электрода рассчитывается как:
(Mg2+/Mg) = 0(Mg2+/Mg) + (0,059 / n) lg[Mg2+]
0(Mg2+/Mg) стандартный электродный потенциал магния, В
[Mg2+] концентрация ионов магнния, моль/л
(Mg2+/Mg) = -2,363В + (0,0...
![В табл. одиннадцать указаны материалы электродов и концентрации ионов металла в растворе электролита[Mе n+] (моль/дм три). Значения стандартных электродных потенциалов металлов приведены](/public/images/library/external/library-detail-hero-book.png)