Условие:
Произведите расчет объемов и энтальпии воздуха и продуктов сгорания.
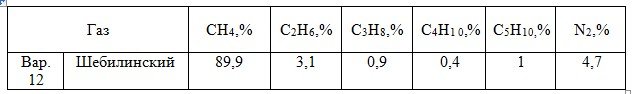
Решение:
1.1 Реакции горения углеводородов:
CH4 +O2 = CO2 +2H2O
C2H6 +3,5O2 = 2CO2 +3H2O
C3H8 +5O2 = 3CO2 +4H2O
C4H10 +6,5O2 = 4CO2 +5H2O
C5H10 +7,5O2 = 5CO2 +5H2O
В общем случае CmHn +(m+n/4)O2 = mCO2 +(n/2)H2O
1.2 Количество кислорода, VО2, нм3/нм3, необходимое для сжигания 1нм3 газообразного топлива составит:
VО2=0,01[(m+n/4) CmHn +0,5 CO + 0,5 H2 +1,5 H2S O2]
VО2=0,01[1СН4+3,5С2Н6+5С3Н8+6,5С4Н10+7,5С5Н10]
VО2=0,01[1∙89,9+3,5∙3,1+5∙0,9+6,5∙0,4+7,5∙1]=1,1535 нм3/нм3
1.3 Количество воздуха, V0, нм3/нм3,требуемое для горения газообразного топлива вычисляю...
