Условие:
В процессе изменения состояния 1 кг газа внутренняя энергия его увеличивается на Δu. При этом над газом совершается работа, равная l. Начальная температура газа –t1, конечное давление p2.
Определить для заданного газа показатель политропы n, начальные и конечные параметры, изменение энтропии Δh. Представить процесс в p-v и T-s – диаграммах. Изобразить также (без расчёта) изобарный, изохорный, изотермический и адиабатный процессы, проходящие через ту же начальную точку, и дать их сравнительный анализ.
m = 1 кг
Δu =-165 кДж/кг
l =245 кДж/кг
t1=2050˚С=2323 К
p2=0,11 Мпа
Вид газа – NH3
Решение:
Для метана NH3 молярная теплоёмкость 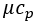 =37,6 Дж/(моль*К)
=37,6 Дж/(моль*К)
молекулярная масса газа, для NН3 ( = 17 г/моль = 0,017 кг/моль)
R= 8,314 Дж/моль*К- газовая постоянная
Найдем газовую постоянную R для NН3
R=R/ = 8,314/0,017 = 489 Дж/(кг*К)
Удельная массовая теплоёмкость СН4:
