Условие:
Реакция 2А + В = 2С протекает в газовой фазе при температуре 298 К и давлении Р = 1,5 атм. Составьте уравнение закона химического равновесия, если начальные количества веществ равны стехиометрическим коэффициентам, продуктов реакции в начальный момент нет. Рассчитайте константу химического равновесия Кр ([р] = 1 атм) и равновесный состав смеси, если известно, что глуби-на химической реакции при этой температуре равна 0,49.
Необходимо вычислить:
1) значение константы равновесия реакции Кр;
2) состав равновесной смеси в молях (пА, пВ, пС);
3) состав равновесной смеси в мольных долях (NА, NВ, NС).
Решение:
Запишем в общем виде закон химического равновесия для данной реакции:
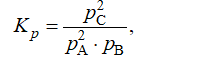
где рА, рВ и рС парциальные давления компонентов равновесной смеси.
По условию начальные количества веществ n0А = 2 моль, n0В = 1 моль и n0С = 0. Пусть к моменту наступления равновесия глубина химической реакции составляет х, т.е. про-реагировало 2х моль вещества А, х моль вещества В и образовалось согласно уравне-нию реакции 2...
